Aunque el tema de la radiactividad, se ha escuchado y leído, sobre la base de algunos acontecimientos ocurridos, desgraciadamente estos son relacionados con accidentes, como el de Chernobil donde hubo un escape de radiación y la sobredosis que sufrieron decenas de pacientes en el año 1996 en Costa Rica, también se habla mucho de la problemática de los desechos radiactivos y desde luego la historia resalta sobre las bombas atómicas utilizadas en la segunda guerra mundial. Pero realmente es poco lo que se conoce del tema. Hace falta conocer los beneficios que causa, los alcances científicos y las precauciones que se debe tener con el manejo de la radiactividad, como lo es el uso adecuado de Isótopos en medicina, más exactamente el medicina nuclear, y es en este punto donde avances como el logrado con el Dicloruro de radio-223 ((Ra-223-Cl2) Alpharadin) como tratamiento a la metástasis ósea.
EL RADIO
El radio, es un elemento químico altamente radiactivo, incluso más que el uranio. Su nombre deriva del término latino, radius, cuyo significado es, rayo. Su símbolo es Ra, y posee un número atómico de 88 que lo coloca en la serie química de los metales alcalinotérreos. Su aspecto es de un metal blanco, el cual se torna de color negro cuando se expone al aire.
El radio fue descubierto en 1898 por M. Curie en la pechblenda (7 toneladas de mineral contienen aproximadamente 1 g de radio). En la corteza representa el % en peso. El elemento fue aislado en 1911 por M. Curie y A. Debierne por electrólisis de una solución de cloruro de radio puro con un cátodo de mercurio; la amalgama se destila en atmósfera de hidrógeno y se obtiene el metal puro. Actualmente se obtiene como bromuro o cloruro, no existiendo cantidades apreciables del elemento aislado. Tanto él como sus sales muestran luminiscencia y por eso se emplean en pinturas oscuras. Emite partículas alfa, beta y rayos gamma y cuando está mezclado con berilio emite neutrones (ver figura 2). Un gramos de 226-Ra (isótopo más común, 1600 años de período de semidesintegración) produce desintegraciones en un segundo, o lo que es lo mismo 1 Bq (Becquerel).
Entre sus características más importantes se tiene la siguiente tabla:
TABLA I. Características generales del Radio.
| Radio | |
| Símbolo químico | Ra |
| Número atómico | 88 |
| Grupo | 2 |
| Periodo | 7 |
| Densidad | 5000 kg/m3 |
| Masa atómica | (226,0254) u u |
| Radio atómico | 215 |
| Punto de fusión | 973 K |
| Calor de fusión | 37 kJ/mol |
El radio, posee un total de 32 isótopos distintos, existiendo cuatro de ellos en la naturaleza. Uno de los isótopos del radio más frecuente y común, es el radio-226, procede de la desintegración del U-238. Así, el Ra-226, se convierte en el isótopo del radio, más duradero pues su periodo de desintegración es de en torno a 1602 años, pasando a partir de ahí, a convertirse en el elemento, radón. El Ra-223, Ra-224, Ra- 226 y Ra-228, se forman a través de desintegración de otros elementos como puede ser el uranio o el torio.
Isótopo 223 Radio… características y sus usos
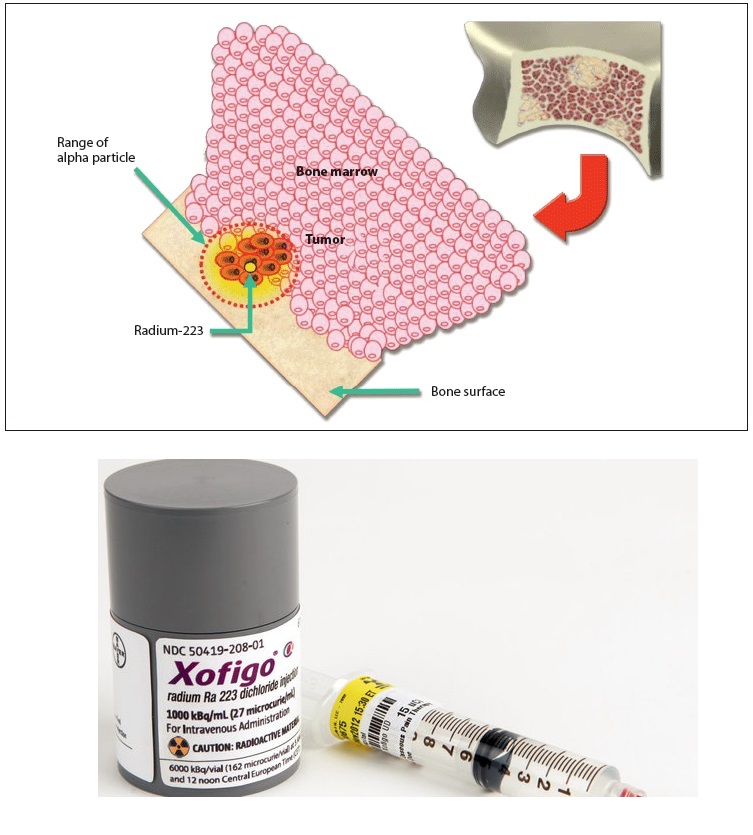
El (223Ra) es un isótopo de radio con un tiempo de semivida de 11,4 días, en contraste con el isótopo común el radio-226, descubierto por los esposos Curie, que tiene una vida media de 1.601 años. El uso principal de radio-223, como un producto radiofarmacéutico para el tratamiento de cánceres metastásicos en el hueso, se aprovecha de su similitud química con calcio, y el corto alcance de la radiación alfa que emite. El (223Ra) ha sido desarrollado por la empresa noruega ALGETA ASA, en una asociación con Bayer®, con el nombre comercial Xofigo (antes Alpharadin), y se distribuye como una solución que contiene cloruro de radio-223 (1.000 Bq / ml), cloruro de sodio, y otros ingredientes para inyección intravenosa. El régimen recomendado es de seis tratamientos de 50 kBq / kg (1,3 Ci por kg), que se repite a intervalos de 4 semanas.
………Si desea conocer mas a fondo las aplicaciones de este elemento radiactivo le recomendamos leer el siguiente articulo.